| 3.5 无机非金属材料组成与晶体结构(8)
2. 层状和架状硅酸盐晶体结构
1)层状硅酸盐晶体结构
层状硅酸盐晶体结构的特点是[SiO4]通过3个顶角上的氧,在二维平面内延伸形成硅氧四面体层,在层内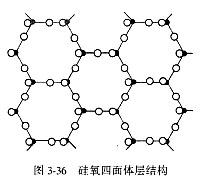 [SiO4]之间形成六元环状,另外一个顶角共同朝一个方向。硅氧四面体层的结构形式如图3-36所示。在层内,[SiO4]顶角上的氧的价键已经饱和,而另一个顶角上的氧是自由氧,价键尚未饱和,需要与其他阳离子(如Mg2+、Al3+、Fe3+、Fe2+等)连接。这些其他离子所形成的配位多面体(八面体)也要构成六元环状。它们之间有2种连接方式:如果八面体以共棱方式相连,但O2-只被2个正离子所共用,这种八面体称为二八面体,也就是说,只有2/3 八面体空隙被正离子填充,[AlO6]就属此种情况。Al3+分配给O2-的静电键强度S=3/6=1/2,每个O2-与2个Al3+连接,占去1价;[SiO4]中Si4+分配给O2-的静电键强度S=4/4=1。其总和等于氧的电荷数,达到了电荷平衡,因此这种结构是稳定的。如果八面体以共棱方式相连,但O2-被3个正离子所共用,这种八面体称为三八面体,也就是说,全部八面体空隙都被正离子填充,[MgO6]就属此种情况。Mg2+分配给O2-的静电键强度S=2/6=1/3,每个O2-与3个Mg2+连接,占去1价;[SiO4]中Si4+分配给O2-的静电键强度S=4/4=1。其总和等于氧的电荷数,达到了电荷平衡,因此这种结构也是稳定的。不管是二八面体还是三八面体,八面体层网络中仍有一些O2-不能与Si4+配位(活性氧),因而剩余电价就要由H+来平衡,所以层状结构中都有OH-出现。 [SiO4]之间形成六元环状,另外一个顶角共同朝一个方向。硅氧四面体层的结构形式如图3-36所示。在层内,[SiO4]顶角上的氧的价键已经饱和,而另一个顶角上的氧是自由氧,价键尚未饱和,需要与其他阳离子(如Mg2+、Al3+、Fe3+、Fe2+等)连接。这些其他离子所形成的配位多面体(八面体)也要构成六元环状。它们之间有2种连接方式:如果八面体以共棱方式相连,但O2-只被2个正离子所共用,这种八面体称为二八面体,也就是说,只有2/3 八面体空隙被正离子填充,[AlO6]就属此种情况。Al3+分配给O2-的静电键强度S=3/6=1/2,每个O2-与2个Al3+连接,占去1价;[SiO4]中Si4+分配给O2-的静电键强度S=4/4=1。其总和等于氧的电荷数,达到了电荷平衡,因此这种结构是稳定的。如果八面体以共棱方式相连,但O2-被3个正离子所共用,这种八面体称为三八面体,也就是说,全部八面体空隙都被正离子填充,[MgO6]就属此种情况。Mg2+分配给O2-的静电键强度S=2/6=1/3,每个O2-与3个Mg2+连接,占去1价;[SiO4]中Si4+分配给O2-的静电键强度S=4/4=1。其总和等于氧的电荷数,达到了电荷平衡,因此这种结构也是稳定的。不管是二八面体还是三八面体,八面体层网络中仍有一些O2-不能与Si4+配位(活性氧),因而剩余电价就要由H+来平衡,所以层状结构中都有OH-出现。
在层状硅酸盐晶体中,又有两层型(1:1型)和三层型(2:1型)之分,前者是由1层[SiO4]+1层[AlO6]/[MgO6]相互交替排列而成,后者是由两层[SiO4]层间夹一层[AlO6] / [MgO6]而形成,整个硅酸盐结构就是以这两层或者三层作为单元,重复堆积而成。每两层或每三层单元内质点之间是化学键结合,很牢固,而单元层之间是依靠分子键或者氢键结合,结合力较弱,很容易沿层间解理,或者在层间渗入水分子。对于实际的硅酸盐晶体,还常常存在离子取代现象,比如[SiO4]中的Si4+被Al3+等取代,八面体层中Al3+也可能被Mg2+或Fe2+等取代,造成电价不平衡,就必然在单元层之间进入其他低价阳离子,如Na+、K+等,以保持电中性。如果该阳离子在层间结合力较弱,就有可能被其他浓度高或者结合力更强的阳离子所交换,这就是粘土类矿物的阳离子交换性质。某些层状矿物还有另外一个特点,就是单元层之间结合力很弱,容易渗入大量水分子。此二特点在蒙脱石中表现得最为突出。
(1)高岭石(1:1型,[SiO4]+[AlO6])
化学式:Al4[Si4O10](OH)8或Al2O3・2SiO2・2H2O,三斜晶系,C1空间群,ao=0.5139nm,bo=0.8932nm,co=0.7371nm,α=91°36',β=104°48',γ=89°54',z = 1。在高岭石结构中(图3-37),离子取代很少,化学组成比较纯净。每两层之间的联系主要是氢键,其结合力要强于分子键,因此单元层之间不容易渗入水分子,可以交换的阳离子容量也小。
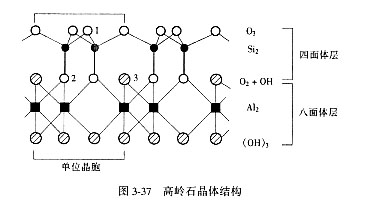
下面用Pauling静电价规则验证结构的稳定性,分别选取标记为1、2和3的三个离子。
1号氧离子跟2个Si4+连接,Si4+与O2-呈四面体配位,所以每个Si4+分配给O2-的静电键强度S = 4/4 = 1。现O2-与2个Si4+连接,所以获得2个静电键,与其电荷数相等,达到静电平衡。
2号氧离子跟1个Si4+和2个Al3+连接,从Si4+获得1个静电键。Al-O呈八面体配位,配位数为6,所以每个Al3+分配给O2-的静电键强度S = 3/6 = 1/2。现有2个Al3+与O2-连接,所以O2-从Al3+也获得1个静电键。2号氧离子从与其配位成键的所有正离子共获得2个静电键,与其电荷数相等,达到静电平衡。
3号氧离子与2个Al3+和1个H+连接,同上,O2-从Al3+获得1个静电键,H+只跟这个氧离子连接,也给它1个静电键,总数为2个静电键,与其电荷数相等,达到静电平衡。
(2)蒙脱石(2:1型,[SiO4]+[AlO6]+[SiO4])
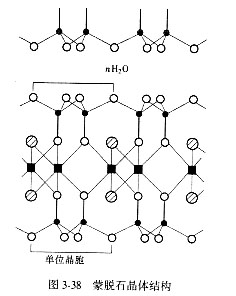
化学式:Al2O3・4SiO2・H2O+nH2O或Al2[Si4O10](OH)2・nH2O,单斜晶系(图3-38),C2/m空间群,ao≈0.523nm,bo≈0.906nm,co可变,z = 2。蒙脱石中容易发生离子取代作用,主要是铝氧八面体中Al3+被Mg2+所取代,为了平衡多余的负电价,在单元层之间就要有其它阳离子M+或M2+进入,取代后实际化学式变为:MgxAl2-x[Si4O10](OH)2・Mx・nH2O。在一定条件下,这些层间阳离子M+或M2+容易被交换出来,因此蒙脱石的阳离子交换容量大。另外蒙脱石的每三层之间结合力弱,很容易渗入水分子,使c轴晶胞参数出现随着渗入水量而变化的现象,因而被称作膨润土。所以,蒙脱石具有阳离子交换容量大和c轴可膨胀的特性。前几年出现了一种制备有机/无机复合纳米材料的新方法――插层方法,就是利用蒙脱石单元层之间结合力弱的特点,在层间插入不同分子(主要是高分子物质)来制备新型纳米复合材料,可以获得很多新的性能、新的材料,如超高吸水率材料或者具有某种电性能的材料,具有良好的应用前景。
|

