| 3.5 无机非金属材料组成与晶体结构(1)
3.5.1 典型结构类型
本节总体要求读者掌握无机材料典型的晶体结构类型,能够对其晶胞进行分析和描述――晶系、基本格子、等同点分析、正负离子配位数(CN±)、晶胞分子数z、质点坐标、四面体和八面体空隙数量、位置及被占据情况、同晶型典型物质及特性,熟记几个典型晶体结构图。
1. 金刚石型结构
金刚石型结构是以金刚石结构作为代表的。金刚石的化学式为C,属立方晶系,基本格子是立方面心格子,空间群符号Fd3m,晶胞参数ao=0.356nm。图3-21是金刚石的晶胞图和投影图,此晶胞中共有8个C原子,分别位于立方面心的所有结点位置和交替分布在立方体内8个小立方体中的4个小立方体的中心。有2套等同点,8个顶角和6个面心的质点属于一套,构成立方面心格子,体内的4个质点属于一套。务必注意,不同套的等同点,必须具有相同的布拉维格子,一个晶胞中只能有一种布拉维格子。在金刚石晶体中,C原子的配位数为4,C-C之间形成共价键。当建立了坐标系之后,就可以确定每个质点的坐标位置,如质点A的坐标为:1/4, 1/4, 3/4,质点B的坐标为:1/2, 1, 1/2,质点C的坐标为:1, 1, 1。这种采用数值化方式描述晶体结构是最规范化的,但以球体堆积的方法来描述晶体结构,则相对直观,有助于理解。为了方便表示晶胞,还可以采用投影图,图3-21中示出了晶胞在(001)面上的投影图,各质点在a轴、b轴方向上的位置,已在投影图中示出,在c轴方向的高度则由数字标出,可以用百分制或者分数表示,比如50或者1/2均表示在c轴方向一半的高度,其余类推。
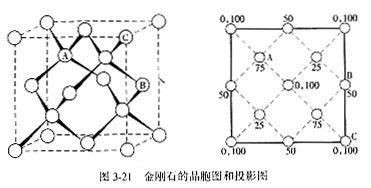
在金刚石晶体中,质点不作紧密堆积,加上C原子质量较轻,所以金刚石的密度较小。由于C-C之间形成很强的共价键,所以金刚石具有非常高的硬度和熔点,其硬度是自然界所有物质中为最高的。它具有很好的导热性能,是由于组成质点单一,有助于声子传导和热辐射。金刚石还具有半导体性能。因此,金刚石常被用作高硬切割材料和磨料以及钻井用钻头、集成电路中散热片和高温半导体材料。
与金刚石属于同一种类型结构的物质有硅、锗、灰锡(a-Sn)、人工合成立方氮化硼(c-BN)等。自然界中存在少量天然金刚石,工业上主要用石墨经高温高压合成得到。
2. 石墨结构
石墨的化学式也是C,属六方晶系,六方原始格子,P63/mmc空间群,ao=0.246nm,co=0.670nm。石墨的结构(图3-22)特征是C原子成层状排列,每一层中C原子排列成六方环状,每个C原子与周围3个C原子成共价键结合,键长0.142nm。层与层之间依靠分子键结合,层间距0.335nm。虚线范围是单位晶胞。石墨的很多性质是与石墨的这种结构特点密不可分的。由于石墨层间结合力较弱,使其容易沿层间解理,有滑腻感,表现出良好的润滑性,在机械工业上作为中低温固体润滑剂。C原子有4个外层电子,但在层内只有3个电子参与成键,多余1个电子可在层内移动,类似于金属中的自由电子,因此,在平行于层的方向具有良好的导电性,可以用作电极和气氛炉的高温发热体,石墨发热体最高使用温度可达2000°C以上。石墨硬度低,易加工,在惰性气氛中熔点很高,可用作高温坩埚。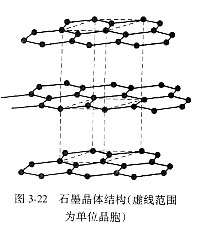
人工合成六方氮化硼(h-BN)与石墨具有相同的结构类型,在石墨晶体结构中,将C原子依次交替换成B原子和N原子,就成了h-BN。它是陶瓷中惟一可以用车、刨、铣、钻进行机加工的陶瓷,可用作高温固体润滑剂,不导电。
金刚石和石墨具有相同的化学组成,但结构类型却绝然不同,这是由于它们的生成热力学条件不同所致。石墨是在高温下生成,而金刚石却是在高温高压条件下生成。我们把化学组成相同的物质,在不同的热力学条件下生成不同的晶体结构的现象,称为同质多晶现象。对于由此而产生的每一种化学组成相同、而结构不同的晶体,称为变体或者多晶形。由于各变体是在不同的热力学条件下形成的,因此当外界条件改变时,各变体之间就要发生结构转变,称为同质多晶转变。后面所要涉及到的许多物质都存在同质多晶现象和同质多晶转变。
与同质多晶相对应的另一个名词是类质同晶,其定义是:物质结晶时,其晶体结构中原有离子或原子的配位位置被介质中性质相似的其他离子或原子所占有,共同组成均匀的、呈单一相的混合晶体,但不引起键性和晶体结构发生质变的现象。比如在地壳中经常发现方解石(CaCO3)和菱镁矿(MgCO3)共生成白云石[(Ca, Mg)CO3],就属于类质同晶现象的一个典型例子。
|

