| 5.7 固溶体生成热力学(1)
从物质的微观结构着眼,固溶体的概念是指组分之间离子(或原子)相互替代关系,但实际上固溶体的生成是大量微观质点运动的统计结果。因此,可以用热力学方法分析和讨论固溶体生成的条件及影响因素。为了简化,设组分A、B之间形成置换固溶体。系统的自由能表示为:
G=U+PV-TS (5-88)
常压下,凝聚系统自由能可写成:
G=U-TS (5-89)
现分别讨论内能U与熵S。
5.7.1. 混合熵
固溶体中溶质在溶剂中的分布是任意的。在一定温度下除了具有温度熵S1外,系统还具有混合熵S2,它是由于溶质和溶剂的混合,溶质原子改变了原来溶剂原子分布规律而产生的。因而,它是结构不规则程度的尺度。由统计力学可知,混合熵是波尔兹曼常数k和热力学几率自然对数的乘积:
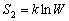 (5-90) (5-90)
式中,W表示原子在固溶体晶格中的可能分布数。设固溶体晶格中结点位置空着,它可容纳N个原子。其中有n个A原子,(N-n)个B原子。A、B原子在固溶体中的可能分布数可表示为:
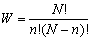 (5-91) (5-91)
代入式(5-90),得
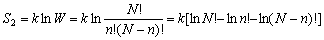 (5-92) (5-92)
根据斯特令公式,当x值很大时,有
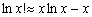 (5-93) (5-93)
则
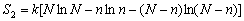 (5-94) (5-94)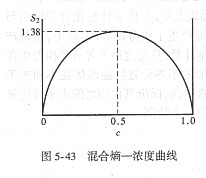
设A原子在固溶体中的原子百分浓度为c,则c=n/N。B原子浓度为(1-c),
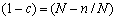 (5-95) (5-95)
代入式(5-94)
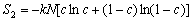 (5-96) (5-96)
由于c和(1-c)都是分数,其对数皆为负数,故S2为正值,即混合熵永远为正值。对于1mol晶体,则kN = R=8.32 J/K。代入(5-96)式可作出S2-c曲线如图5-43所示。
式(5-96)和图5-42表明:A、B之间形成固溶体从熵的变化判断是有利的。但是,事实上并非任何两个组分都能形成固溶体,还必须考虑生成固溶体时晶体内能的变化。
|

